0 تا 100 معتبرسازی فریزدرایر (خشک کن انجمادی) : اصول ، مراحل و چالش ها
- Morteza Aghajani
- دستهبندی نشده
معتبرسازی فریزدرایر یکی از موارد مهم در صنعت داروسازی میباشد. فریزدرایرها (Freeze Dryers) یا خشککنهای انجمادی، تجهیزات حیاتی در صنایع دارویی، غذایی و بیوتکنولوژی هستند که برای حذف رطوبت از مواد حساس به حرارت استفاده میشوند. معتبرسازی فریزدرایر، فرآیندی است که اطمینان حاصل میکند این دستگاهها به طور مداوم و مطابق با استانداردهای کیفیت و ایمنی عمل میکنند. در این مقاله، به بررسی جامع اصول، مراحل و چالشهای معتبرسازی فریزدرایر میپردازیم.
معتبرسازی فریزدرایر یکی از مراحل کلیدی در صنایع داروسازی، بیولوژیکی و غذایی است که به منظور تضمین عملکرد صحیح و پایدار دستگاه و تولید محصولات با کیفیت عالی انجام میشود. این فرآیند به دلایل مختلفی اهمیت ویژهای دارد که در ادامه به برخی از مهمترین آنها اشاره خواهیم کرد.
تضمین کیفیت محصول یکی از دلایل اصلی اهمیت معتبرسازی فریزدرایر (Validation) است. در فرآیند فریزدرایینگ، حفظ کیفیت، خلوص و اثربخشی محصول نهایی از اهمیت بالایی برخوردار است. معتبرسازی فریزدرایر تضمین میکند که دستگاه به درستی تنظیم شده و قادر به انجام فرآیند خشک کردن انجمادی مطابق با استانداردهای تعیینشده است. این فرآیند باعث میشود که محصول نهایی با خواص فیزیکی و شیمیایی مطلوب تولید شود و از ایجاد هرگونه تغییرات ناخواسته در ساختار آن جلوگیری گردد. همچنین، این فرآیند باعث جلوگیری از آسیب به مواد حساس دارویی و بیولوژیکی میشود که میتواند تأثیرات منفی بر روی اثربخشی درمانی آنها داشته باشد.
رعایت الزامات قانونی نیز از دیگر دلایل اهمیت معتبرسازی فریزدرایر (خشک کن انجمادی) است. بسیاری از صنایع، به ویژه در حوزه داروسازی و بیوتکنولوژی، ملزم به رعایت مقررات سختگیرانهای مانند GMP (Good Manufacturing Practice) هستند. این مقررات نیازمند معتبرسازی تجهیزات و فرآیندها به منظور اطمینان از کیفیت و ایمنی محصولات تولیدی است. عدم رعایت این الزامات ممکن است منجر به رد صلاحیت تجهیزات و حتی جریمههای قانونی شود. معتبرسازی فریزدرایر (Validation) به شرکتها کمک میکند تا از مطابقت کامل با این الزامات قانونی اطمینان حاصل کنند و فرآیندهای تولیدی آنها مورد تأیید مقامات نظارتی قرار گیرد.
کاهش خطرات یکی از دیگر جنبههای حیاتی معتبرسازی فریزدرایر است. فرآیند خشک کردن انجمادی، به دلیل پیچیدگیهای خاص خود، ممکن است در صورت عدم نظارت و کنترل دقیق به خطرات مختلفی منجر شود. معتبرسازی فریزدرایر به شناسایی و کاهش این خطرات کمک میکند. در این فرآیند، تمامی مراحل از نصب دستگاه گرفته تا عملکرد آن در شرایط عملیاتی بررسی میشود تا اطمینان حاصل شود که دستگاه به درستی کار میکند و هیچگونه خطری برای کیفیت محصول نهایی وجود ندارد. این کار به جلوگیری از مشکلاتی مانند آسیب به محصول، عدم توازن دما یا فشار، و مشکلات دیگر که میتوانند تأثیر منفی بر روی کیفیت محصول داشته باشند، کمک میکند.
افزایش بهرهوری یکی از مزایای مهم معتبرسازی فریزدرایر (Validation) است. این فرآیند با بهینهسازی عملکرد دستگاه، میتواند به افزایش بهرهوری و کاهش هزینههای تولید کمک کند. معتبرسازی فریزدرایر اطمینان میدهد که دستگاه به طور بهینه عمل میکند و از هدررفت منابع و زمان جلوگیری میشود. با توجه به اینکه در صنایع داروسازی و بیوتکنولوژی هرگونه تأخیر یا نقص در فرآیند تولید میتواند هزینهبر باشد، معتبرسازی کمک میکند تا دستگاه با بیشترین کارایی عمل کرده و عملکرد بهتری داشته باشد.
در نتیجه، معتبرسازی فریزدرایر به عنوان یک ابزار حیاتی در تضمین کیفیت، ایمنی و بهرهوری در فرآیند تولید محصولات دارویی، بیولوژیکی و غذایی اهمیت زیادی دارد. این فرآیند نه تنها کمک میکند که محصولات نهایی با کیفیت مطلوب تولید شوند، بلکه از رعایت مقررات قانونی و کاهش خطرات احتمالی نیز اطمینان میدهد. به علاوه، معتبرسازی با بهینهسازی عملکرد دستگاهها، هزینهها را کاهش داده و بهرهوری را افزایش میدهد، که این امر در نهایت به بهبود عملکرد کلی صنعت کمک میکند.
اصول معتبرسازی فریزدرایر
معتبرسازی فریزدرایر (خشک کن انجمادی) یکی از مراحل حیاتی در تأمین کیفیت محصولات دارویی، بیولوژیکی و غذایی است که به منظور تضمین عملکرد صحیح و پایدار دستگاه در تمامی مراحل تولید و فرآیندهای حساس انجام میشود. معتبرسازی فریزدرایر بر پایه اصول خاصی استوار است که از آن جمله میتوان به مستندسازی، آزمایش، تکرارپذیری و مدیریت انحرافات اشاره کرد.
مستندسازی یکی از اصول اساسی معتبرسازی فریزدرایر است. در تمامی مراحل معتبرسازی، از نصب دستگاه تا عملیات تولید، باید تمامی اقدامات و تستها به طور دقیق و کامل مستند شوند. این مستندات شامل دستورالعملها، گزارشهای آزمایشگاهی، دادههای فنی، کالیبراسیون سنسورها، تنظیمات دستگاه و نتایج تستها میشود. مستندسازی دقیق برای اطمینان از انطباق با الزامات نظارتی و مقررات صنعتی، نظیر GMP و FDA، ضروری است و به عنوان مرجع برای بازرسیها و ارزیابیهای آینده عمل میکند.
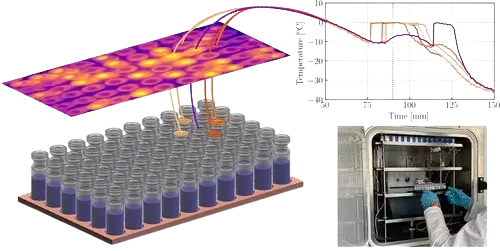
آزمایشها بخش مهم دیگری از فرآیند معتبرسازی فریزدرایر (خشک کن انجمادی) هستند. این آزمایشها به منظور اثبات عملکرد صحیح و پایدار دستگاه در شرایط مختلف عملیاتی انجام میشوند. آزمایشهایی مانند اندازهگیری دما، فشار، خلأ، نرخ انجماد و عملکرد کندانسور باید تحت شرایط دقیق و استاندارد انجام شده و دادههای حاصل از آنها با مشخصات تعیینشده مقایسه شوند. این آزمایشها باید بر اساس پروتکلهای معتبر و با استفاده از تجهیزات دقیق صورت گیرند تا اطمینان حاصل شود که دستگاه قادر به تولید محصولاتی با کیفیت بالا است.
تکرارپذیری یکی دیگر از اصول معتبرسازی فریزدرایر است. نتایج آزمایشها باید قابل تکرار باشند تا اطمینان حاصل شود که فریزدرایر در تمامی چرخههای کاری خود توانایی انجام فرآیند فریزدرایینگ را با دقت و ثبات داشته و محصولات نهایی دارای کیفیت ثابت و قابل پیشبینی خواهند بود. این امر به ویژه در صنایع دارویی و بیولوژیکی که هرگونه تغییر در فرآیند تولید میتواند تأثیرات منفی بر کیفیت محصول داشته باشد، اهمیت زیادی دارد.
انحرافات از دیگر اصولی هستند که باید در فرآیند (خشک کن انجمادی) معتبرسازی فریزدرایر به دقت ثبت و بررسی شوند. هرگونه انحراف از مشخصات تعیینشده، اعم از تغییر در دما، فشار، نرخ خلأ یا عملکرد دستگاه، باید شناسایی و مستند شود. این انحرافات ممکن است به دلایل مختلفی از جمله خرابی تجهیزات، تغییرات در شرایط محیطی یا تنظیمات نادرست دستگاه رخ دهند. ثبت و بررسی این انحرافات برای انجام اقدامات اصلاحی و جلوگیری از تأثیرات منفی آنها بر فرآیند تولید بسیار حیاتی است.
در نهایت، اصول معتبرسازی فریزدرایر بهطور کلی به منظور اطمینان از عملکرد صحیح، ایمن و پایدار دستگاه در تمامی مراحل تولید و فرآیندهای حساس طراحی شدهاند. این اصول نه تنها تضمینکننده کیفیت محصولات نهایی هستند، بلکه از بروز مشکلات غیرمنتظره در فرآیند تولید و انطباق با الزامات نظارتی جلوگیری میکنند.
مراحل معتبرسازی فریزدرایر
معتبرسازی فریزدرایر معمولاً شامل مراحل زیر است:
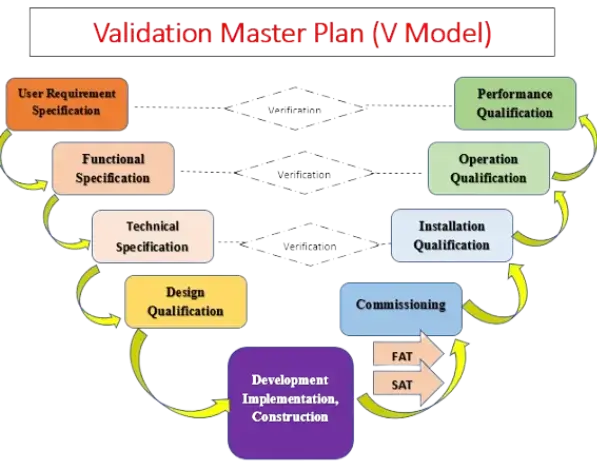
1. طراحی معتبرسازی (DQ):
احراز صلاحیت طراحی (Design Qualification – DQ) فریزدرایر یکی از مراحل حیاتی در فرآیند ولیدیشن تجهیزات داروسازی است که تضمین میکند طراحی دستگاه مطابق با استانداردهای صنعتی، نیازهای تولید و الزامات کیفی باشد. این فرآیند بر اساس بررسی دقیق مستندات طراحی، مشخصات فنی و تطابق آنها با الزامات GMP، مقررات FDA و EU-GMP انجام میشود. در این مرحله، تمامی جنبههای عملکردی و ایمنی فریزدرایر ارزیابی شده و تأیید میشود که طراحی آن توانایی اجرای فرآیند لیوفیلیزاسیون را با دقت و یکنواختی بالا دارد.
بررسی نقشههای فنی، انتخاب متریالهای مورد استفاده در ساخت، طراحی سیستمهای کنترل دما و فشار، توزیع یکنواخت حرارت در سینیها، نرخ کندانس بخار، ظرفیت پمپ وکیوم و توانایی تجهیزات در حفظ شرایط استریل از مهمترین مواردی است که در احراز صلاحیت طراحی بررسی میشود. مستندات DQ باید شامل تحلیل نیازمندیهای طراحی، محاسبات مهندسی، شبیهسازیهای عملکردی و تطابق طراحی با دستورالعملهای بینالمللی باشد.
این مرحله پیشنیازی برای اجرای موفق IQ (احراز صلاحیت نصب) و OQ (احراز صلاحیت عملیاتی) است و در صورت اجرای صحیح، از مشکلات احتمالی در مراحل بعدی جلوگیری میکند. مستندسازی دقیق در این بخش، نقش کلیدی در کاهش ریسکهای عملیاتی، بهبود کیفیت محصولات نهایی و افزایش بهرهوری فریزدرایر دارد. اجرای صحیح DQ نهتنها ایمنی و کارایی دستگاه را تضمین میکند، بلکه موجب کاهش هزینههای تعمیر و نگهداری در آینده خواهد شد. از سوی دیگر، این فرآیند به تولیدکنندگان کمک میکند تا از تطابق تجهیزات خود با استانداردهای جهانی اطمینان حاصل کرده و در بازرسیهای قانونی بدون مشکل عمل کنند. یک DQ دقیق و جامع، مسیر را برای فرآیندهای ولیدیشن هموار ساخته و از بروز مشکلات در تولید داروهای حساس جلوگیری میکند.
2. نصب معتبرسازی (IQ):
احراز صلاحیت نصب (Installation Qualification – IQ) فریزدرایر یکی از مراحل اساسی در فرآیند تضمین کیفیت تجهیزات دارویی و صنعتی است که اطمینان حاصل میکند دستگاه مطابق با مشخصات فنی و استانداردهای مورد نیاز نصب شده است. این مرحله شامل بررسی مستندات فنی، تأیید صحت نصب قطعات، بررسی ارتباطات الکتریکی و مکانیکی، تطبیق دستگاه با دستورالعملهای تولیدکننده و ثبت تمامی اطلاعات مرتبط میشود.
احراز صلاحیت IQ فریزدرایر تضمین میکند که تمامی اجزا، از جمله محفظه خلأ، کندانسور، پمپ خلأ، سنسورها و کنترلرها، به درستی در جای خود قرار گرفته و مطابق با استانداردهای GMP، FDA و EU نصب شدهاند. همچنین بررسی چکلیستهای مربوط به تجهیزات جانبی، کالیبراسیون سنسورها و عملکرد اولیه سیستم از جمله مواردی است که در این مرحله انجام میشود. مستندسازی دقیق فرآیند IQ برای ردیابی مشکلات احتمالی در مراحل بعدی مانند احراز صلاحیت عملکردی (OQ) و احراز صلاحیت فرآیندی (PQ) بسیار حیاتی است.
این فرآیند توسط تیمهای مهندسی و تضمین کیفیت انجام میشود و شامل اجرای تستهای اولیه برای تأیید عملکرد صحیح اجزای فریزدرایر میباشد. علاوه بر این، تمامی مدارک و گزارشهای مربوط به نصب باید مطابق با الزامات بازرسیهای داخلی و خارجی نگهداری شوند. عدم اجرای صحیح احراز صلاحیت IQ میتواند منجر به مشکلات عملکردی، عدم تطابق با الزامات نظارتی و حتی آسیب به محصول نهایی شود. بنابراین، اجرای این فرآیند با دقت و رعایت استانداردهای معتبر جهانی، یکی از الزامات حیاتی در صنعت داروسازی، زیستفناوری و صنایع غذایی است.
3. عملکرد معتبرسازی (OQ):
احراز صلاحیت عملیاتی (Operational Qualification – OQ) فریزدرایر یکی از مراحل کلیدی در فرآیند تأیید تجهیزات دارویی و صنعتی است که اطمینان حاصل میکند دستگاه پس از نصب، مطابق با استانداردهای عملکردی مورد انتظار عمل میکند.
در این مرحله، تمامی پارامترهای کلیدی عملکردی مانند دما، فشار، خلأ، نرخ انجماد، ظرفیت کندانسور و پاسخ سیستم کنترلی تحت شرایط استاندارد و چالشبرانگیز آزمایش میشوند. احراز صلاحیت OQ فریزدرایر شامل تستهای دقیق برای تأیید صحت عملکرد اجزای مختلف از جمله سیستمهای خنککننده، گرمکننده، پمپ خلأ، شیرهای کنترلی، سنسورها و نرمافزار کنترلی است.
این فرآیند معمولاً با اجرای تستهای تکرارشونده در شرایط مختلف عملیاتی انجام شده و تمام دادهها مستندسازی میشوند تا اطمینان حاصل شود که دستگاه به طور پایدار و قابل پیشبینی عمل میکند. علاوه بر این، کالیبراسیون سنسورها و بررسی دقت قرائتها نقش مهمی در احراز صلاحیت عملیاتی دارند. اجرای صحیح OQ تضمین میکند که فریزدرایر میتواند در محدوده مشخصات طراحیشده کار کند و در صورت بروز هرگونه انحراف، اقدامات اصلاحی انجام شود. این مرحله همچنین ارتباط مستقیمی با الزامات GMP، FDA و سایر استانداردهای نظارتی دارد و عدم رعایت آن میتواند باعث رد صلاحیت دستگاه در بازرسیهای قانونی شود.
احراز صلاحیت عملیاتی باید توسط تیمهای مهندسی و تضمین کیفیت با استفاده از پروتکلهای دقیق و از پیش تعیینشده انجام شود. پس از تکمیل این مرحله، دادههای بهدستآمده مبنای ورود به احراز صلاحیت فرآیندی (PQ) قرار میگیرند که عملکرد دستگاه را در شرایط واقعی تولید بررسی میکند. بنابراین، OQ نقش حیاتی در تأیید عملکرد صحیح فریزدرایر ایفا کرده و از بروز مشکلات در مراحل تولید و کنترل کیفیت جلوگیری میکند.
4. عملکرد فرآیند معتبرسازی (PQ):
احراز صلاحیت کارایی (Performance Qualification – PQ) فریزدرایر آخرین مرحله از فرآیند تأیید این تجهیزات حیاتی در صنایع دارویی و زیستفناوری است که عملکرد دستگاه را در شرایط واقعی تولید مورد ارزیابی قرار میدهد.
در این مرحله، فریزدرایر با بارگذاری محصولات واقعی یا شبیهسازیشده آزمایش شده و تمامی پارامترهای کلیدی مانند یکنواختی توزیع دما، کنترل فشار، نرخ خشک شدن، عملکرد کندانسور و پایداری خلأ تحت شرایط عملیاتی مورد بررسی قرار میگیرند. احراز صلاحیت PQ تضمین میکند که فریزدرایر قادر به تولید محصولات با کیفیت و تکرارپذیری بالا است و عملکرد آن مطابق با الزامات GMP، FDA و سایر استانداردهای بینالمللی میباشد.
این مرحله شامل اجرای چرخههای متعدد فریزدرایینگ و بررسی دادههای بهدستآمده برای اطمینان از صحت عملکرد دستگاه در مواجهه با سناریوهای واقعی تولید است. مستندسازی دقیق نتایج، تحلیل دادهها و بررسی میزان تطابق با استانداردهای تعیینشده نقش مهمی در این فرآیند دارند.
در صورت مشاهده هرگونه انحراف در پارامترهای عملکردی، اقدامات اصلاحی انجام شده و تستها مجدداً اجرا میشوند تا پایداری و قابلیت اطمینان سیستم تأیید شود. احراز صلاحیت کارایی نهتنها کیفیت محصول نهایی را تضمین میکند، بلکه از بروز مشکلاتی مانند ناپایداری فرآیند، افزایش زمان خشک شدن، کاهش کیفیت محصول و عدم انطباق با مقررات جلوگیری میکند.
این مرحله معمولاً توسط تیمهای تضمین کیفیت و مهندسی فرآیند انجام شده و موفقیت آن شرط لازم برای استفاده از فریزدرایر در تولید محصولات حساس دارویی و بیولوژیکی است. علاوه بر این، دادههای حاصل از PQ برای بهینهسازی فرآیند فریزدرایینگ و افزایش بهرهوری تولید مورد استفاده قرار میگیرند. بنابراین، احراز صلاحیت کارایی گام نهایی و حیاتی در تأیید عملکرد فریزدرایر است که از کیفیت و ایمنی محصولات نهایی اطمینان حاصل میکند.
5. احراز صلاحیت مجدد (بعد از تعمیرات)
(Requalification – RQ)
احراز صلاحیت مجدد (Requalification – RQ) فریزدرایر پس از انجام تعمیرات یا تغییرات اساسی، یکی از مراحل حیاتی در تضمین عملکرد صحیح و پایدار این دستگاه در صنایع دارویی و زیستفناوری است. این فرآیند شامل اجرای تستهای کیفی و عملیاتی برای تأیید این موضوع است که فریزدرایر پس از تعمیرات همچنان مطابق با الزامات طراحی و استانداردهای نظارتی مانند GMP و FDA کار میکند. احراز صلاحیت مجدد معمولاً زمانی ضروری میشود که قطعات مهمی مانند پمپ خلأ، کندانسور، سیستم کنترل دما، شیرهای کنترلی یا نرمافزار دستگاه تعویض، تعمیر یا بهروزرسانی شده باشند.
این فرآیند شامل سه مرحله اصلی یعنی احراز صلاحیت نصب مجدد (IQ)، احراز صلاحیت عملیاتی مجدد (OQ) و احراز صلاحیت کارایی مجدد (PQ) است تا تمامی جنبههای عملکردی دستگاه مورد بررسی قرار گیرند. انجام تستهای دما، فشار، خلأ، ظرفیت کندانسور و یکنواختی توزیع حرارت در این مرحله ضروری است. تمامی دادههای بهدستآمده باید مستندسازی شده و با مقادیر قبلی مقایسه شوند تا از صحت عملکرد دستگاه اطمینان حاصل گردد.
در صورتی که نتایج تستها نشاندهنده هرگونه انحراف از معیارهای تعیینشده باشد، اقدامات اصلاحی انجام شده و آزمایشها مجدداً اجرا میشوند. احراز صلاحیت مجدد نهتنها عملکرد بهینه فریزدرایر را تضمین میکند، بلکه از بروز مشکلات احتمالی در تولید، کاهش کیفیت محصول و عدم انطباق با مقررات جلوگیری میکند.
این فرآیند باید توسط تیمهای تخصصی مهندسی و تضمین کیفیت انجام شده و گزارشهای مربوطه برای بازرسیهای داخلی و خارجی آماده شوند. علاوه بر این، احراز صلاحیت مجدد میتواند به بهینهسازی فرآیندهای عملیاتی و افزایش طول عمر دستگاه کمک کند. بنابراین، اجرای دقیق RQ پس از هرگونه تغییر یا تعمیرات اساسی، یک الزام ضروری برای حفظ کارایی، ایمنی و کیفیت محصولات تولیدی در صنایع حساس محسوب میشود.

